基于相位和幅值联合重建的多激发高清扩散成像(中文,English)
钱晨1, 王孜1, 张心林1,施博轩1, 姜博宇2, 陶冉2, 李敬3, 葛玉伟3, 康泰山4, 林建忠4, 郭迪5, 屈小波1*
1 厦门大学,电子科学系,福建等离子体与磁共振重点研究实验室,健康医疗大数据国家研究院,中国,厦门.
2 联影医疗, 中国,上海.
3 鑫高益医疗设备股份有限公司, 中国,宁波.
4 厦门大学附属中山医院,放射系,中国,厦门.
5 厦门理工学院,计算机与信息工程学院, 中国, 厦门.
引用
Chen Qian, Zi Wang, Xinlin Zhang, Boxuan Shi, Boyu Jiang, Ran Tao, Jing Li, Yuwei Ge, Taishan Kang, Jianzhong Lin, Di Guo, and Xiaobo Qu, A paired phase and magnitude reconstruction for advanced diffusion-weighted imaging, IEEE Transactions on Biomedical Engineering, DOI: 10.1109/TBME.2023.3288031, 2023.
研究背景
磁共振扩散成像被广泛用于脑科学研究[1]和临床疾病诊断[2]。传统基于单激发平面回波序列采集的扩散图像面临分辨率低,图像畸变大的问题[3], 难以满足临床应用和科学研究需求。多激发交错式平面回波技术可提高扩散图像空间分辨率和减少畸变,但其重建会受到各次激发间运动相位干扰[4],产生严重运动伪影。
主要研究内容与结果
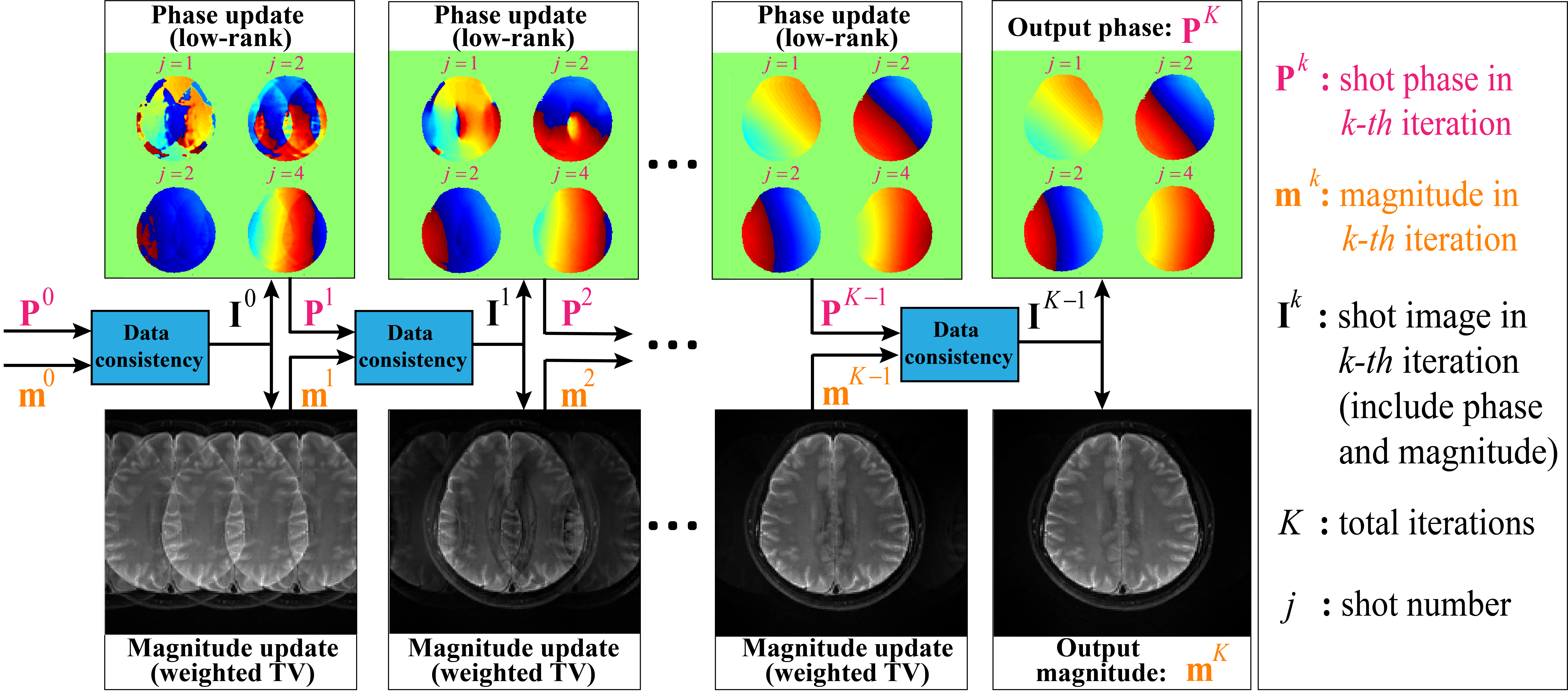
本工作致力于实现基于多激发交错式平面回波序列的高清高b值扩散图像的重建,利用相位和幅值的互补双域先验,提出基于相位和幅值联合更新的重建框架PAIR(图1)。其中k空间低秩约束来源于各次激发运动相位的光滑导致的共轭对称性[5],用于矫正运动伪影。图像域加权总变分约束来自多b值和多扩散方向图像之间的相似结构信息,用以进一步提高重建图像信噪比。这对互补先验有助于准确的相位和无伪影幅度图像重建。

图1. 基于相位和幅值联合更新的重建框架PAIR实现高保真的相位和无伪影幅度图像重建。
实验表明,PAIR可以有效利用多b值图像提供的结构先验,实现边缘结构保护的图像去噪,提高重建信噪比并保护边缘细节。
图2.
PAIR使用不同的总变分重建结果对比。(b)(c)为PAIR使用不同参数的加权总变分重建,其中权重从高信噪比的非扩散图像(a)中提取。(d)为PAIR使用传统无加权总变分重建。
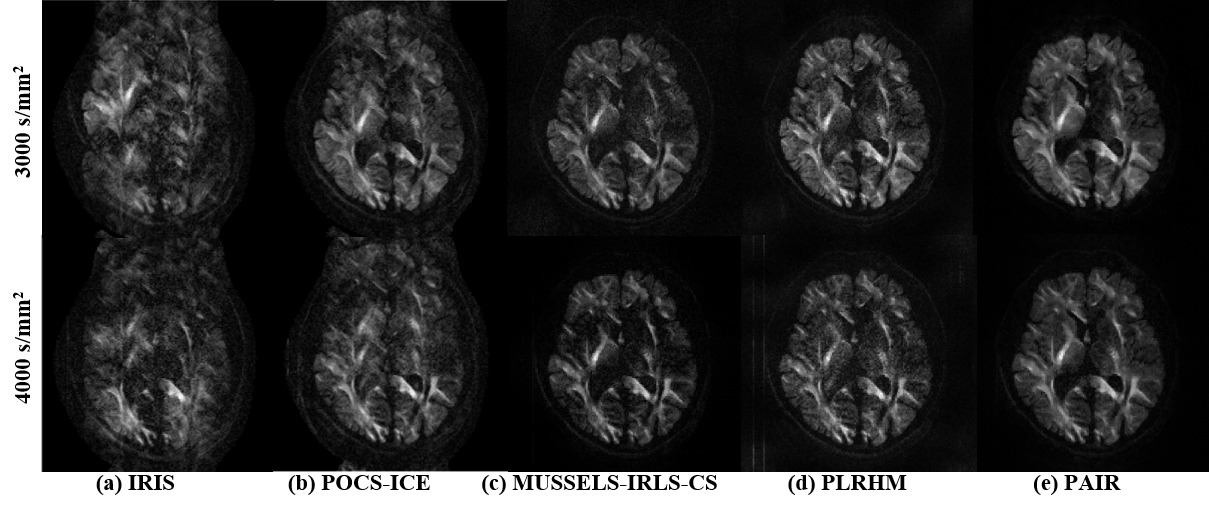
模拟和体内数据的结果表明[6-8],PAIR在超高b值(3000/4000 s/mm2)的重建场景下,可以很好地去除各次激发间的运动伪影(8次激发),并显著抑制噪声。
图3. 超高b值的八次激发扩散图像重建。在上海的联影3.0T设备采集,分辨率1.5*1.5 mm2。
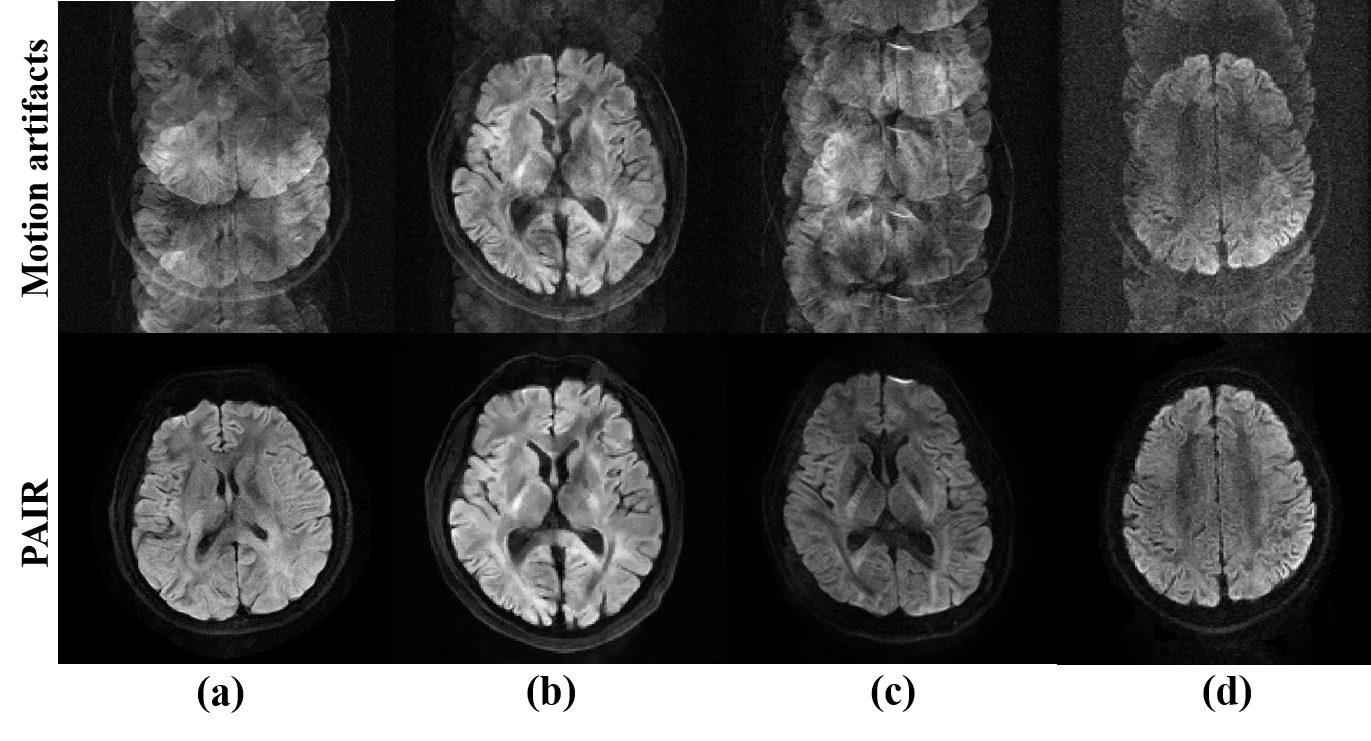
PAIR在多中心数据(在北京采集的飞利浦3.0T, 在上海采集的联影3.0T, 在厦门采集的飞利浦3.0T, 在宁波采集的鑫高益GreenMR Serenity 1.5T)表现鲁棒,均能实现高保真的图像重建。
图4. PAIR重建多中心多设备商数据,b值均为1000
s/mm2。从左到右,分别为在北京采集的飞利浦3.0T数据,8次激发,分辨率1.0*1.0 mm2;在上海采集的联影3.0T数据,4次激发,分辨率1.5*1.5
mm2;在厦门采集的飞利浦3.0T数据,4次激发,分辨率1.2*1.2 mm2;在宁波采集的鑫高益1.5T数据,4次激发。
代码
可通过计算感知实验室云脑成像平台(https://csrc.xmu.edu.cn/CloudBrain.html)使用PAIR重建方法[10, 11],(测试账号: radiologist1, 密码:
radiologist1!)。
致谢
本工作得到国家自然科学基金(62122064、61971361和61871341)、福建省自然科学基金(2021J011184)、厦门大学校长基金(20720220063)和厦门大学南强拔尖人才计划的资助。
参考文献
[1] D. K. Jones, “Diffusion MRI”. Oxford University Press, 2010.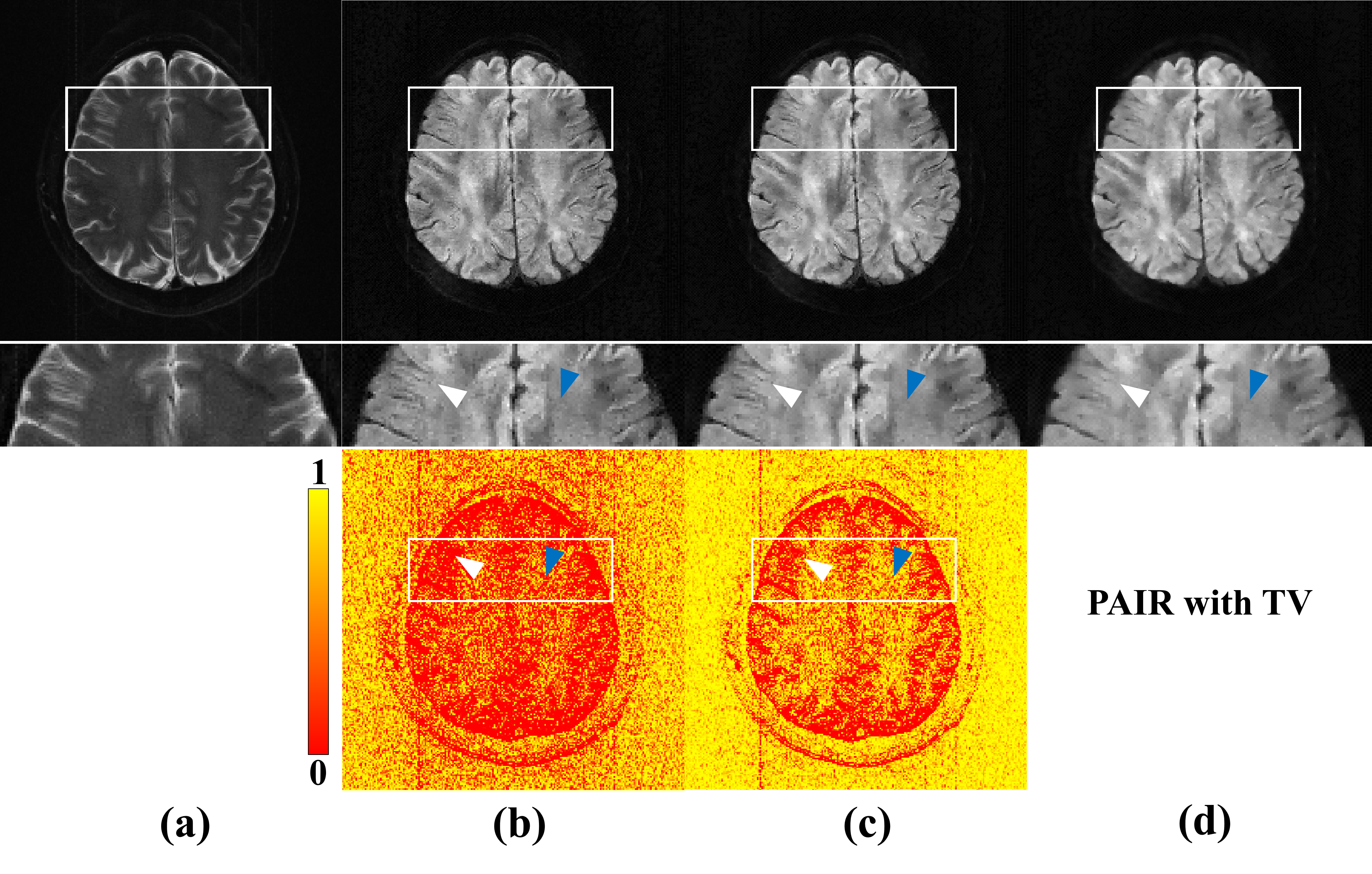
[2] M. G. Lansberg, G. W. Albers, C. Beaulieu, and M. P. Marks, “Comparison of diffusion-weighted MRI
and CT in acute stroke,” Neurology, vol. 54, no. 8, pp. 1557-1561, 2000.
[3] G. C. Baxter, A. J. Patterson, R. Woitek, I. Allajbeu, M. J. Graves, and F. Gilbert, “Improving the
image quality of DWI in breast cancer: comparison of multi-shot DWI using multiplexed sensitivity
encoding to conventional single-shot echo-planar imaging DWI,” The British Journal of Radiology, vol.
94, no. 1119, 20200427, 2021.
[4] A. W. Anderson and J. C. Gore, “Analysis and correction of motion artifacts in diffusion weighted
imaging,” Magnetic Resonance in Medicine, vol. 32, no. 3, pp. 379-87, 1994.
[5] J. P. Haldar, “Low-rank modeling of local k-space neighborhoods (LORAKS) for constrained MRI,” IEEE
Transaction on Medical Imaging, vol. 33, no. 3, pp. 668-681, 2013.
[6] H. Guo, X. Ma, Z. Zhang, B. Zhang, C. Yuan, and F. Huang, “POCS‐enhanced inherent correction of
motion‐induced phase errors (POCS‐ICE) for high‐resolution multishot diffusion MRI,” Magnetic Resonance
in Medicine, vol. 75, no. 1, pp. 169-180, 2016.
[7] M. Mani, M. Jacob, D. Kelley, and V. Magnotta, “Multi‐shot sensitivity‐encoded diffusion data
recovery using structured low‐rank matrix completion (MUSSELS),” Magnetic Resonance in Medicine, vol.
78, no. 2, pp. 494-507, 2017.
[8] M. Mani, H. K. Aggarwal, V. Magnotta, and M. Jacob, “Improved MUSSELS reconstruction for
high-resolution multi-shot diffusion weighted imaging,” Magnetic Resonance in Medicine, vol. 83, no. 6,
pp. 2253-2263, 2020.
[9] Y. Huang et al., “Phase-constrained reconstruction of high-resolution multi-shot diffusion weighted
image,” Journal of Magnetic Resonance, vol. 312, 106690, 2020.
[10] Q. Yang, Z. Wang, K. Guo, C. Cai, and X. Qu, “Physics-driven synthetic data learning for biomedical
magnetic resonance: The imaging physics based data synthesis paradigm for artificial intelligence,” IEEE
Signal Processing Magazine, vol. 40, no. 2, pp. 129-140, 2023.
[11] Y. Zhou et al., “XCloud-pFISTA: A medical intelligence cloud for accelerated MRI,” in 43rd Annual
International Conference of the IEEE Engineering in Medicine and Biology Society (EMBC), 2021, pp.
3289-3292.